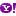Molte reazioni chimiche spontanee liberano energia, come avviene per esempio nella combustione, nella dissoluzione di idrossido di sodio in acqua e moltissimi altri casi.
Alcune reazioni invece hanno la caratteristica di assorbire una certa quantità di calore per compiersi. Un esempio è la dissoluzione del nitrato di ammonio in acqua, sfruttato nelle borse di ghiaccio istantaneo impiegate in pronto soccorso. Anche l'assorbimento del gas ammoniaca in acqua è una reazione fortemente endotermica e per questo largamente impiegata nell'industria del freddo.
Anche in questo caso la materia prima viene riciclata all'interno di un circuito sigillato. In uno scambiatore interno alla camera da refrigerare avviene la reazione, dopodiché la miscela acqua/ammoniaca viene convogliata in un bollitore esterno dove viene scaldata e fatta evaporare. La fonte di calore in genere è una resistenza elettrica o una fiamma. Il vapore è quindi condensato in una apposita serpentina dove, a causa della diversa velocità di condensazione delle due molecole avviene la separazione, ed il ciclo può ricominciare.
Piccoli frigoriferi che sfruttano il principio descritto, detti ad assorbimento, si possono trovare nelle stanze degli alberghi o negli uffici, dove è ne apprezzata la caratteristica di estrema silenziosità, dovuta all'assenza del compressore. Un ulteriore vantaggio è legato alla possibilità di funzionamento con una semplice fonte di calore, per cui essere alimentato con gas combustibile, per esempio nei camper. Il motivo per cui questo meccanismo non rimpiazza il sistema a compressore è dovuto ai maggiori costi di produzione.



 Rispondi Citando
Rispondi Citando

 ?
?